Hệ thần kinh giao cảm: Cơ chế, điều trị và mối liên quan với suy tim
Hệ thần kinh giao cảm có thể gây hàng loạt tác động tim mạch, bao gồm tăng tần số tim và tăng sức co bóp cơ tim. Ngược lại, hệ thần kinh phó giao cảm (thông qua dây thần kinh lang thang) làm giảm tần số tim.
1. Cơ chế và mối liên quan giữa hệ thần kinh giao cảm và tim
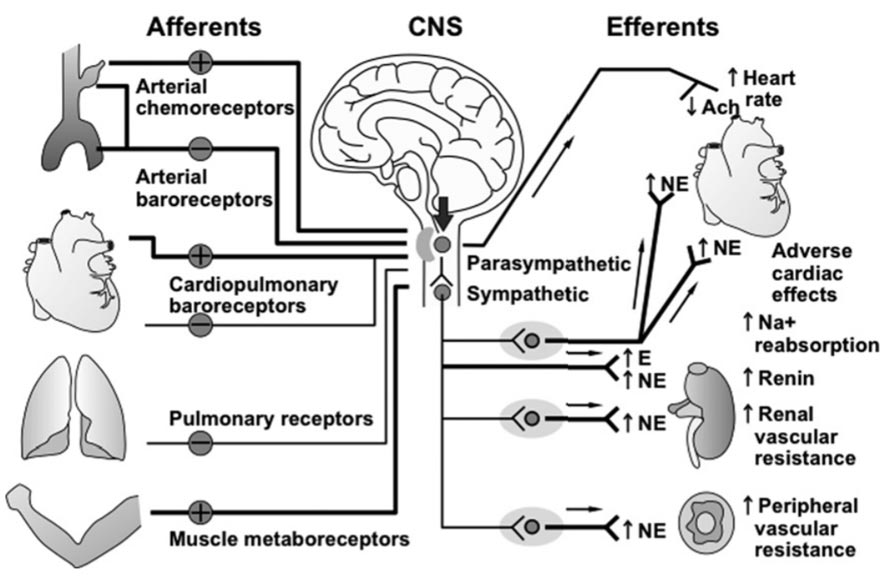
Nhiều nghiên cứu cơ bản và lâm sàng đã chứng tỏ có sự tăng hoạt hóa hệ thần kinh giao cảm và/hoặc giảm xung thần kinh phó giao cảm trong suy tim (Hình 1) [1]. Nói cách khác, suy tim được xem là một tình trạng điển hình cho rối loạn và mất cân bằng chức năng thần kinh tự chủ.
>> Xem thêm: Tăng huyết áp là gì?
Khi bệnh nhân xảy ra rối loạn chức năng tâm thu, cơ thể cố gắng bù trừ bằng tăng cường hệ thần kinh lẫn hệ thể dịch nhằm nỗ lực bảo toàn cung lượng tim [2]. Hệ thần kinh giao cảm đáp ứng bằng cách tăng hoạt tính giao cảm, đồng thời giảm hoạt tính phó giao cảm.
Trong khi đó, hệ thể dịch đáp ứng bằng cách tăng tiết một số hormone như trục renin-angiotensin-aldosterone [3]. Với rối loạn chức năng tâm trương, mặc dù hiện ít có bằng chứng về cơ chế sinh lý bệnh hơn nhưng sự tăng hoạt giao cảm cũng đã có bằng chứng góp phần vào sự tiến triển rối loạn chức năng tâm trương thất trái và liên quan đến tăng nguy cơ tim mạch [4].
Tìm hiểu kỹ hơn cơ chế cường giao cảm ở bệnh nhân suy tim chủ yếu do sự mất điều hòa các cung phản xạ, cụ thể là cung phản xạ ức chế giao cảm tim mạch (thụ thể áp lực ở động mạch) bị ức chế, mất khả năng làm nhiệm vụ thông thường của chúng là ức chế giao cảm, trong khi đó các cung phản xạ kích thích giao cảm tim (thụ thể hóa học ở động mạch và phản xạ giao cảm tim hướng tâm) đều bị kích hoạt quá mức.
Ngoài những cơ chế chính này, gần đây một số cơ quan khác cũng được tìm ra tham gia vào hiện tượng cường giao cảm ở bệnh nhân suy tim, trong đó phổi đóng vai trò khá quan trọng. Nghiên cứu ghi nhận có sự giảm nhạy cảm thụ thể phổi và tăng hoạt động điều biến phản xạ tim - phổi mà bản chất là một dạng cung phản xạ kích thích giao cảm tim làm tăng áp lực đổ đầy thất (Hình 1) [1].
Ở người bị suy tim, một nghiên cứu khác cho thấy sự tăng tốc độ lan truyền các chất chuyển hóa của norepinephrine và epinephrine ở tĩnh mạch cảnh trong, đồng thời có sự tương quan chặt giữa chu chuyển norepinephrine ở não và tốc độ lan truyền norepinephrine tim [5].
Điều này gợi ý rằng hiện tượng kích hoạt các neuron tiết noradrenergic từ thân não là yếu tố trung gian điều hòa hoạt tính giao cảm và sự bất thường ở trung ương có khả năng là nguyên nhân dẫn đến kích hoạt giao cảm quá mức tại tim.

>> Xem thêm: Hệ thần kinh giao cảm và mối liên quan với bệnh mạch vành
2. Vai trò của hệ thần kinh phó giao cảm
Bên cạnh hệ thần kinh giao cảm, không thể không kể đến vai trò của một thành phần đối lập nhưng thống nhất để kiểm soát hoạt động cơ thể là hệ phó giao cảm. Cả đầu tận cảm giác của dây giao cảm và phó giao cảm hướng tâm chi phối tim đều là các thụ thể sức căng, do đó chúng bị kích hoạt khi tim giãn ra trong tình huống suy tim.
Tuy nhiên, khi buồng tim giãn, sợi giao cảm tăng phát xung mạnh hơn, dẫn đến sự ức chế tương đối trương lực và phản xạ phó giao cảm [6]. Trong suy tim tâm trương, tim không có hiện tượng giãn, do vậy cơ chế dẫn đến giảm hoạt tính phó giao cảm vẫn còn đang được nghiên cứu thêm.

3. Phương pháp hạn chế bệnh suy tim phổ biến
3.1 Sử dụng thuốc
Dựa trên hai cơ chế sinh lý bệnh này, nhiều thử nghiệm đã cố gắng tập trung vào hai đích đến nhằm hạn chế tiến triển suy tim: Ức chế hoạt tính giao cảm và kích thích hoạt tính phó giao cảm.
Thuốc ức chế beta
Là nhóm thuốc đầu tiên và chủ đạo đã được chấp thuận dùng trong mục đích này từ sớm vì khả năng ức chế hoạt tính giao cảm [7]. Lợi ích kết cục lâm sàng trên bệnh nhân suy tim được chứng minh với các đại diện như bisoprolol (nghiên cứu CIBIS-II), metoprolol (nghiên cứu MERIT-HF), carvedilol (nghiên cứu COPERNICUS) và nebivolol (nghiên cứu SENIORS) [8-11].
Việc sử dụng thuốc ức chế beta dài hạn giúp cải thiện chức năng thất trái, trì hoãn hoặc đảo ngược một phần hiện tượng tái cấu trúc thất trái, giảm nguy cơ nhập viện do suy tim và cải thiện sống còn.
Nhóm thuốc ức chế thụ thể alpha-1
Ngoài thụ thể beta, hệ thần kinh giao cảm adrenergic còn có các thụ thể alpha.Tuy nhiên, nỗ lực trị liệu bằng việc ức chế thụ thể alpha-1 với prazosin (nghiên cứu Veteran Administrative Cooperative Study) hay doxazosin (nghiên cứu ALLHAT) đều đưa đến kết cục xấu hơn cho bệnh nhân suy tim và vì vậy hướng tiếp cận này được xem là không phù hợp [12, 13].
Nhóm thuốc ức chế thụ thể alpha-2 trung ương
Thuốc ức chế alpha-2 trung ương clonidine có thể làm giảm trương lực giao cảm tim-thận hiệu quả, tuy nhiên cần thêm các thử nghiệm lâm sàng lớn để đánh giá lợi ích về kết cục trên bệnh nhân suy tim [14].
Một điều thú vị là có thể giảm hoạt tính giao cảm không nhờ thuốc mà thông qua hoạt động thể lực. Những bằng chứng gần đây cho thấy luyện tập có thể giúp giảm thêm xung giao cảm ở bệnh nhân suy tim đang điều trị với ức chế beta, như vậy có khả năng hiệp đồng cùng nhau hạn chế tác động có hại của cường giao cảm [15].
Các cơ chế được đề xuất để lý giải hiện tượng này là (1) lấy lại sự kiểm soát các cung phản xạ thụ thể áp lực và hóa học ở động mạch, (2) giảm cung lượng giao cảm từ não, (3) điều chỉnh các bất thường ở thần kinh trung ương, (4) tăng biểu hiện các chất chống oxi hóa và ức chế con đường oxi hóa ở trung ương [16].
3.2. Phương pháp điện học
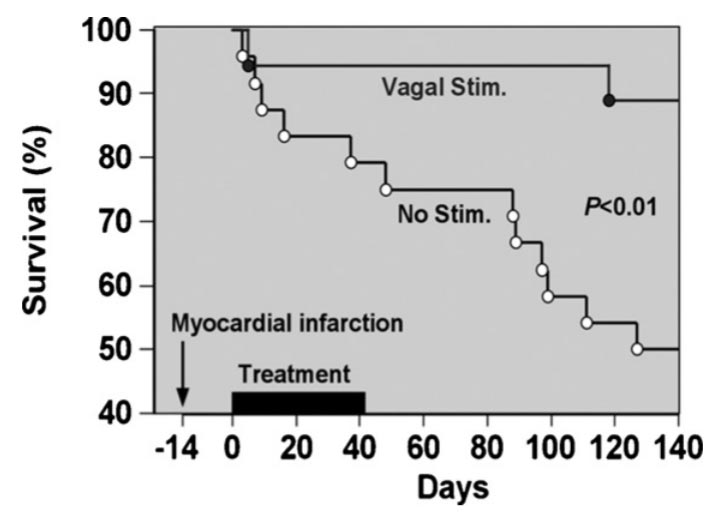
Hướng điều trị thứ hai được đề xuất thay vì ức chế hệ thần kinh giao cảm là kích thích phó giao cảm bằng điện học. Trên mô hình chuột suy tim sau nhồi máu cơ tim, kích thích dây thần kinh lang thang đưa đến sự cải thiện có ý nghĩa động học thất trái và giảm tử vong từ 50% xuống còn 14% (p <0.01) sau 140 ngày theo dõi (Hình 2) [17].
Trong một nghiên cứu khác, kích thích phó giao cảm khi phối hợp với sử dụng thuốc ức chế beta cải thiện chức năng thất trái tốt hơn chỉ dùng ức chế beta đơn thuần [18].
>> Xem thêm: Tại sao và nên tập thể dục như thế nào là tốt cho tim mạch?
Tóm lại, trong suy tim, có sự rối loạn chức năng thần kinh tự chủ, cụ thể là tăng hoạt tính hệ thần kinh giao cảm và giảm hoạt tính hệ thần kinh phó giao cảm. Các dữ liệu hiện tại nhấn mạnh tầm quan trọng của việc ức chế hệ thần kinh giao cảm trong điều trị suy tim thông qua sử dụng thuốc ức chế beta và hoạt động thể lực.
Tài liệu tham khảo.
-
Kishi T. Heart failure as an autonomic nervous system dysfunction. J Cardiol. 2012 Mar;59(2):117-22
-
Triposkiadis F, Karayannis G, Giamouzis G, Skoularigis J, Louridas G, Butler J. The sympathetic nervous system in heart failure: physiology, pathophysiology, and clinical implications. J Am Coll Cardiol 2009;54:1747—62
-
Dzau VJ, Colucci WS, Hollenberg NK, Williams GH. Relation of the renin—angiotensin—aldosterone system to clinical state in congestive heart failure. Circulation 1981;63:645—51
-
Grassi G, Seravalle G, Quarti-Trevano F, Dell’Oro R, Arenare F, Spaziani D, Mancia G. Sympathetic and baroreflex cardiovascular control in hypertension-related left ventricular dysfunction. Hypertension 2009;53:205—9
-
Floras JS. Sympathetic nervous system: clinical implications of an updated model. J Am Coll Cardiol 2009;54:375—85
-
Schwarts PJ, Ferrari GM. Sympathetic-parasympathetic interaction in health and disease: abnormalities and relevance in heart failure. Heart Fail Rev 2011;16:101—7
-
Hunt SA, Abraham WT, Chin MH, Feldman AM, Francis GS, Ganiats TG, Jessup M, Konstam MA, Mancini DM, Michl K, Oates JA, Rahko PS, Silver MA, Stevenson LW, Yancy CW, et al. ACC/AHA 2005 Guideline Update for the Diagnosis and Management of Chronic Heart Failure in the Adult: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Update the 2001 Guidelines for the Evaluation and Management of Heart Failure): developed in collaboration with the American College of Chest Physicians and the International Society for Heart and Lung Transplantation: endorsed by the Heart Rhythm Society. Circulation 2005;112:e154—235.
-
The Cardiac Insufficiency Bisoprolol Study II (CIBIS-II): a randomised trial. Lancet. 1999 Jan 2;353(9146):9-13. PMID: 10023943
-
MERIT-HF Study Group. Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet 1999;353:2001—7
-
Packer M, Fowler MB, Roecker EB, Coats AJ, Katus HA, Krum H, Mohacsi P, Rouleau JL, Tendera M, Staiger C, Holcslaw TL, Amann-Zalan I, DeMets DL. Carvedilol prospective randomized cumulative survival (COPERNICUS) study group. Effect of carvedilol on the morbidity of patients with severe chronic heart failure: results of the carvedilol prospective randomized cumulative survival (COPERNICUS) study. Circulation 2002;106:2194-9
-
Flather MD, Shibata MC, Coats AJ, Van Veldhuisen DJ, Parkhomenko A, Borbola J, Cohen-Solal A, Dumitrascu D, Ferrari R, Lechat P, Soler-Soler J, Tavazzi L, Spinarova L, Toman J, Böhm M, Anker SD, Thompson SG, Poole-Wilson PA; SENIORS Investigators. Randomized trial to determine the effect of nebivolol on mortality and cardiovascular hospital admission in elderly patients with heart failure (SENIORS). Eur Heart J. 2005 Feb;26(3):215-25
-
Cohn JN, Archibald DG, Ziesche S, Franciosa JA, Harston WE, Tristani FE, Dunkman WB, Jacobs W, Francis GS, Flohr KH. Effect of vasodilator therapy on mortality in chronic congestive heart failure. Results of a veterans administration cooperative study. N Engl J Med 1986;314:1547-52
-
ALLHAT Collaborative Research Group. Major cardiovascular events in hypertensive patients randomized to doxazosin vs chlorthalidone: the antihypertensive and lipid-lowering treatment to prevent heart attack trial (ALLHAT). JAMA 2000;283:1967-75
-
Giles TD, Thomas MG, Quiroz A, Rice JC, Plauche W, Sander GE. Acute and short-term effects of clonidine in heart failure. Angiology 1987;38:537-48
-
Fraga R, Franco FG, Roveda F, de Matos LN, Braga AM, Rondon MU, Rotta DR, Brum PC, Barretto AC, Middlekauff HR, Negrao CE. Exercise training reduces sympathetic nerve activity in heart failure patients treated with carvedilol. Eur J Heart Fail 2007;9:630-6
-
Gao L, Wang W, Liu D, Zucker IH. Exercise training normalizes sympathetic outflow by central antioxidant mechanisms in rabbits with pacing-induced chronic heart failure. Circulation 2007;115:3095-102
-
Li M, Zheng C, Sato T, Kawada T, Sugimachi M, Sunagawa K. Vagal nerve stimulation markedly improves long-term survival after chronic heart failure in rats. Circulation 2004;109:120-4
-
Sabbah HN, Imai M, Zaretsky A, Rastogi S, Wang M, Jiang A. Therapy with vagus nerve electrical stimulation combined with beta-blockade improves left ventricular systolic function in dogs with heart failure beyond that seen with beta-blockade alone. Eur J Heart Fail 2007;6(Suppl. 1):114
 Các ứng dụng di động theo dõi sức khoẻ cho người tăng huyết áp
Các ứng dụng di động theo dõi sức khoẻ cho người tăng huyết áp Công thức nấu ăn cho người tăng huyết áp: Thực đơn 7 ngày
Công thức nấu ăn cho người tăng huyết áp: Thực đơn 7 ngày 4 tác động của tăng huyết áp đến sức khỏe tinh thần cần lưu ý
4 tác động của tăng huyết áp đến sức khỏe tinh thần cần lưu ý Tăng huyết áp và giấc ngủ: Mức độ ảnh hưởng, biến chứng và phòng ngừa
Tăng huyết áp và giấc ngủ: Mức độ ảnh hưởng, biến chứng và phòng ngừa Tình dục và tăng huyết áp có mối liên quan và mức độ ảnh hưởng ra sao?
Tình dục và tăng huyết áp có mối liên quan và mức độ ảnh hưởng ra sao? Giải pháp quản lý tăng huyết áp tại nơi làm việc đơn giản và hiệu quả
Giải pháp quản lý tăng huyết áp tại nơi làm việc đơn giản và hiệu quả Chi tiết về huyết áp kẹt: Mức độ nguy hiểm và hướng dẫn phòng ngừa
Chi tiết về huyết áp kẹt: Mức độ nguy hiểm và hướng dẫn phòng ngừa Người huyết áp cao nên ăn gì và kiêng gì? Lối sống hiện đại ảnh hưởng tới tăng huyết áp như thế nào?
Người huyết áp cao nên ăn gì và kiêng gì? Lối sống hiện đại ảnh hưởng tới tăng huyết áp như thế nào? Hiểu rõ chỉ số huyết áp và nguyên nhân tăng huyết áp ở giới trẻ
Hiểu rõ chỉ số huyết áp và nguyên nhân tăng huyết áp ở giới trẻ8445_400x230.png) Kiểm soát chỉ số huyết áp và tần số tim tại nhà với 10 cách đơn giản
Kiểm soát chỉ số huyết áp và tần số tim tại nhà với 10 cách đơn giản8266_400x230.png) Tần số tim là gì? Chỉ số tần số tim bao nhiêu là bình thường?
Tần số tim là gì? Chỉ số tần số tim bao nhiêu là bình thường?5067_400x230.png) 7 cách quản lý huyết áp tại nhà có thể bạn chưa biết
7 cách quản lý huyết áp tại nhà có thể bạn chưa biết
Đánh giá nguy cơ bệnh
Chỉ cần 5 phút để đánh giá nguy cơ bệnh lý của bạn. Giúp bạn xử trí kịp thời.
Bạn muốn đánh giá nguy cơ bệnh nào ?
- Bệnh đái tháo đường
- Bệnh tiền đái tháo đường
- Bệnh lý tim mạch
- Bệnh lý tuyến giáp


